Tavla perjodika
It-Tavla perjodika tal-elementi kimiċi hija metodu tabulari użat biex jintwerew l-elementi kimiċi. Għalkemm jeżistu prekursuri għal din it-tavla, l-invenzjoni tagħha hija ġeneralment kreditata lill-kimiku Russu Dmitri Mendeleev fl-1869. Mendeleev xtaq li it-tavla turi t-tendenzi rikurrenti ("perjodiċi") fil-proprjetajiet tal-elementi. Id-dehra tat-tavla ġiet irfinuta u estiża matul iż-żmien, hekk kif elementi ġodda ġew skoperti, u mudelli teoretiċi ġodda ġew żviluppati biex l-imġiba kimika tiġi spjegata.
It-tavla perjodika issa tinstab kullimkien fid-dixxiplina akkademika tal-kimika, tipprovdi struttura estremament utli biex jiġu kklassifikati, issistemati u ikkumparati il-ħafna forom differenti tal-imġiba kimika. It-tavla ukoll sabet applikazzjoni fil-fiżika, bijoloġija, inġenjerija, u l-industrija. L-istandard kurrenti tat-tavla fih 118-il element.
Dehra tat-Tavla perjodika
[immodifika | immodifika s-sors]| Grupp | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||
| Perjodu | ||||||||||||||||||||
| 1 | 1 H |
2 He | ||||||||||||||||||
| 2 | 3 Li |
4 Be |
5 B |
6 C |
7 N |
8 O |
9 F |
10 Ne | ||||||||||||
| 3 | 11 Na |
12 Mg |
13 Al |
14 Si |
15 P |
16 S |
17 Cl |
18 Ar | ||||||||||||
| 4 | 19 K |
20 Ca |
21 Sc |
22 Ti |
23 V |
24 Cr |
25 Mn |
26 Fe |
27 Co |
28 Ni |
29 Cu |
30 Zn |
31 Ga |
32 Ge |
33 As |
34 Se |
35 Br |
36 Kr | ||
| 5 | 37 Rb |
38 Sr |
39 Y |
40 Zr |
41 Nb |
42 Mo |
43 Tc |
44 Ru |
45 Rh |
46 Pd |
47 Ag |
48 Cd |
49 In |
50 Sn |
51 Sb |
52 Te |
53 I |
54 Xe | ||
| 6 | 55 Cs |
56 Ba |
57 La |
* |
72 Hf |
73 Ta |
74 W |
75 Re |
76 Os |
77 Ir |
78 Pt |
79 Au |
80 Hg |
81 Tl |
82 Pb |
83 Bi |
84 Po |
85 At |
86 Rn | |
| 7 | 87 Fr |
88 Ra |
89 Ac |
* * |
104 Rf |
105 Db |
106 Sg |
107 Bh |
108 Hs |
109 Mt |
110 Ds |
111 Rg |
112 Cn |
113 Nh |
114 Fl |
115 Mc |
116 Lv |
117 Ts |
118 Og | |
| * Lantanojdi | 58 Ce |
59 Pr |
60 Nd |
61 Pm |
62 Sm |
63 Eu |
64 Gd |
65 Tb |
66 Dy |
67 Ho |
68 Er |
69 Tm |
70 Yb |
71 Lu | ||||||
| ** Attinojdi | 90 Th |
91 Pa |
92 U |
93 Np |
94 Pu |
95 Am |
96 Cm |
97 Bk |
98 Cf |
99 Es |
100 Fm |
101 Md |
102 No |
103 Lr | ||||||
| Metalli alkalini | Metalli alkalini ta' l-art | Lantanojdi | Attinojdi | Metalli tal-blokka d |
| Metalli tal-blokka p | Semimetalli | Non-Metalli | Aloġeni | Gassijiet nobbli |
Leġenda għall-kuluri tan-numri atomiċi:
- L-elementi nnumrati bil-blu huma likwidi f' T = 298 K e p = 1 bar;
- dawk bl-aħdar huma gassijiet f' T = 298 K e p = 1 bar;
- dawk bl-iswed huma solidi f' T = 298 K e p = 1 bar;
- dawk bl-aħmar huma artifiċjali u m'humiex naturalment preżenti fuq id-Dinja (huma kollha solidi f' T = 298 K e p = 1 bar). It-teknezju hu preżenti fi kwantitajiet minimi fil-minjieri ta' l-uranju u fil-ġganti ħomor.
- dawk bil-griż għadhom ma ġewx skoperti.
Arranġament
[immodifika | immodifika s-sors]L-arranġament tat-Tavla Perjodika juri l-propjetajiet kimiċi rikurrenti ("perjodiċi"). L-elementi huma mniżżlin skont il-piż atomiku tagħhom (i.e. in-numru ta' protoni fin-nukleju atomiku). Il-fillieri huma rranġati biex l-elementi bi propjetajiet simili jinstabu fl-istess kolonni vertikali ("gruppi"). Skont it-teoriji tal-konfigurazzjoni elettronika ġo l-atomi tal-Mekkanika kwantistika, kull filliera oriżżontali ("perjodu") fit-tavla tikkorrrispondi għal kif inhi mimlija l-qoxra kwantistka bl-elettroni. Il-perjodi jitwalu aktar ma tinżel l-isfel fit-tavla, li jiġbru l-elementi fi blokok s- , p- , d- and f- biex jirriflettu l-konfigurazzjoni eletronika tagħhom.
Fi twavel stampati, kull element hu normalment imniżżel bis-simbolu u n-numru atomiku tiegħhu; ħafna verżjonijiet tat-tavla ukoll iniżżlu il-piż atomiku tal-element u informazzjoni oħra, bħall-konfigurazzjoni elettronika, elettronegattività u l-akbar numru tal-Valenza komuni.
Wara l-2016, it-tavla fiha 118 elementi kimiċi li l-iskoperti tagħhom ġew ikkonfermati. 94 minnhom jinstabu naturalmant fid-Dinja, u l-oħrajn huma sintetiċi li ġew prodotti artifiċjalment f'aċċeleraturi tal-materja. L-elementi 43 (teknezju), 61 (promezju), 93 (nettunju) u 94 (plutonju) m'għandhomx iżotopi stabbli u ġew skoperti għall-ewwel darba sintekikalment; imma, imbagħad ġew skoperti f'ammonti żgħar fid-Dinja bħala prodotti ta' proċessi naturali.
Perjodiċità tal-propjetajiet kimiċi
[immodifika | immodifika s-sors]Il-valur maġġuri tat-tavla perjodika hu l-abilità li tbassar il-propjetajiet kimiċi t'element skont il-pożizzjoni tiegħhu fit-tavla. Għandu jiġi nnutat illi l-propjetajiet ivarjaw differentament meta timxi vertikalment mal-kolonni tat-tavla, milli meta timxi oriżżontalment mal-fillieri.
Gruppi u perjodi
[immodifika | immodifika s-sors]- Grupp tat-tavla perjodika hu kolonna vertikali fit-tavla perjodika tal-elementi.
Il-gruppi huma meqjusal-aktar metodu importanti biex jiġu klassifikati l-elementi. F'xi gruppi, l-elementi għandhom propjetajiet simili ħafna u juru tendenzi fil-propjetajiet hekk kif tinżel l-isfel fil-grupp — dawn il-gruppi għandhom tendenza li jiġu mogħtija ismijiet trivjali (mhux sistematiċi) , e.ż. il-metalli alkalini, l-metalli alkalini tal-art, l-aloġeni u l-gassijiet nobbli. Xi gruppi oħrajn fit-tavla perjodika juru inqas similiritajiet u/jew tendenzi vertikali (pereżempju Gruppi 14 and 15), u dawn m'għandhomx ismijiet trivjali u jiġu rriferuti sempliċiment bin-numru tal-grupp tagħhom.
- Perjodu tat-tavla perjodika hu filliera oriżżontali fit-tavla perjodika tal-elementi.
Għalkemm il-gruppi huma l-aktar mod komuni biex jiġu klassifikati l-elementi , hemm xi reġjuni tat-tavla perjodika fejn it-tendenzi oriżżontali u s-similiritajiet fil-propjetajiet huma aktar sinjifikanti mit-tendenzi tal-gruppi vertikali. Dan jista' jkun veru fil-blokka d (jew "Metalli Tranżizzjonali"), u speċjalment għall-blokka f , fejn il-lantanojdi u l-attinojdi jiffurmaw żewġ serje oriżżontali sostanzjali t'elementi.
Tendenzi perjodiċi tal-gruppi
[immodifika | immodifika s-sors]Teoriji moderni fuq l-istruttura atomika tal-Mekkanika kwantistika jispjegaw it-tendenzi tal-gruppi billi jipproponu illi l-elementi fl-istess grupp għandhom l-istess konfigurazzjoni elettronika fil-qxur tal-valenza tagħhom , illi hi l-aktar fattur importanti responsabbli għall-propjetajiet simili tagħhom.
Elementi fl-istess grupp ukoll juru tendenzi fir-radju atomiku, enerġija tal-joniżżazzjoni u l-elettronegattività tagħhom. Minn fuq s'isfel f'kwalunkwe grupp, ir-radji atomiċi tal-elementi jiżdiedu. Minħabba li hemm aktar livelli tal-enerġija mimlijin ,l-elettroni jinstabu aktar 'il bogħod min-nukleju. Minn fuq,kull element suċċessiv għandu enerġija tal-joniżżazzjoni iżgħar minħabba li hu aktar faċli li tneħħi elettron minħabba li l-elettroni huma inqas issikati. Ukoll, grupp għandu tnaqqis fl-elettronegattività minn fuq s'isfel minħabba li d-distanza bejn l-elettroni tal-valenza u n-nukleju tkun qed tiżdied.
Tendenzi perjodiċi tal-perjodi
[immodifika | immodifika s-sors]Elementi fl-istess perjodu ukoll juru tendenzi fir-radju atomiku, enerġija tal-joniżżazzjoni, affinità għall-elettroni u fl-elettronegattività tagħhom. Hekk kif timxi mix-xellug għal-lemin f'perjodu , ir-radju atomiku normalment jonqos. Dan jiġri minħabba li kull element suċċessiv għandu proton miżjud u elettron li jġiegħel l-elettron ikun miġbud iktar viċin lejn in-nukleju. Dan it-tnaqqis fir-radju atomiku ukoll jikkawża żieda fl-enerġija tal-joniżżazzjoni meta timxi mix-xellug għal-lemin tal-perjodu. Aktar m'element ikun issikat , aktar tkun l-enerġija li jkun hemm bżonn biex tneħħi elettron. Ukoll, l-elettronegattività tiżdied bl-istess manjiera bħall-enerġija tal-joniżżazzjoni minħabba fl-ammont ta' ġibda imposta fuq l-elettroni min-nukleju. L-affinità għall-elettroni ukoll għandha tendenza f'perjodu. Il-metalli (fix-xellug tal-perjodu) ġeneralment ikollhom inqas affinità għall-elettroni min-Non-metalli (fil-lemin tal-perjodu) bl-eċċezjoni tal-gassijiet nobbli.
Eżempji
[immodifika | immodifika s-sors]Gassijiet nobbli
[immodifika | immodifika s-sors]L-elementi kollha tal-grupp 18 (gassijiet nobbli), għandhom il-qxur tal-valenza tagħhom mimlijin. Dan ifisser li m'għandhomx bżonn jirreaġixxu ma' elementi oħra biex jimlew il-qoxra tagħhom, u huma allura inqas reattivi minn gruppi oħrajn. L-Elju u n-Neon huma l-aktar elementi inerti fost il-gassijiet nobbli, minħabba li r-reattività, f'dan il-grupp, tiżdied bil-perjodi: hu possibbli li ġġiegħel l-gassijiet nobbli t-tqal jirreaġixxu minħabba li għandhom qxur tal-elettroni akbar. Imma, r-reattività tagħhom tibqa baxxa.
Aloġeni
[immodifika | immodifika s-sors]Fil-grupp 17, magħruf bħala l-aloġeni, l-elementi għandhom elettron wieħed biss nieqes mill-qoxra tal-elettroni. Allura, f'reazzjonijiet kimiċi għandhom it-tendenza li jġibu l-elettroni (it-tendenza li ġġib l-elettroni hi msejħa elettronegattività). Din il-propjetà hi l-aktar evidenti għal-Fluworu (l-aktar element elettronegattiv fit-tavla kollha), u jnaqqas maż-żieda ta' kull perjodu.
Bħala riżultat, l-aloġeni kollha jiffurmaw aċidi mal-Idroġenu, bħal fl-Aċidu Idrofluworiku, Aċidu Idrokloriku, Aċidu Idrobromiku u fl-Aċidu Idrojodiku, kollha fil-forma HX. L-aċidità tagħhom tiżdied b'perjodu akbar, pereżempju, bir-rigward għall-Jodju u l-Fluworu, minħabba li jone kbir ta' I− hu aktar stabbli f'soluzzjoni minn jone żgħir ta' F−, hemm inqas volum fejn iċ-ċarġ jista' jkun dispers.
Metalli tranżizzjonali
[immodifika | immodifika s-sors]Għall-metalli tranżizzjonali (Gruppi 3 sa 12), tendenzi oriżżontali matul il-perjodi huma ħafna drabi importanti daqs it-tendenzi vertikali hekk kif tinżel l-isfel matul il-gruppi;id-differenzi bejn il-gruppo maġenb xulxin huma normalment mhux drammatiċi. Ir-reazzjonijiet tal=metalli tranżizzjonali normalment jinvolvu speċi koordinati.
Lantanojdi u Attinojdi
[immodifika | immodifika s-sors]Il-propjetajiet kimiċi tal-lantanojdi(elementi 57–71) u tal-attinojdi (elementi 89–103) huma aktar simili għal xulxin milli tal-metalli tranżizzjonali , u biex tissepara taħlita tagħhom hu veru diffiċli.Dan hu importanti fil-purifikazzjoni kimika tal-Uranju li jikkonċerna l-enerġija nukleari.
Struttura tat-Tavla Perjodika
[immodifika | immodifika s-sors]Id-determinant primarju tal-propjetajiet kimiċi t'element huwa il-konfigurazzjoni elettronika tiegħhu , partikularment l-elettroni fil-qoxra tal-valenza. Pereżempju, kwalunkwe atomi b'egħrba elettroni tal-valenza li jokkupaw l-orbital p ser jeżibixxu xi similarità. It-tip t'orbital li fih jinstabu l-elettroni ta' barra t'element jiddeterminaw il-blokka li fihaa jappartjeni. In-numru t'elettroni tal-valenza jiddetermina l-familja, jew grupp li lilu l-element jappartjeni.
In-numru totali ta' qxur elettroniċi li l-atomu jkollu jiddetermina l-perjodu li lilu jappartjeni. Kull qoxra hija diviża f' sottoqxur differenti, li meta n-numru atomiku jiżdied jiġu mimlija b'din l-ordni (Prinċipju Aufbau):
| Sottoqoxra: | S | G | F | D | P |
| Perjodu | |||||
| 1 | 1s | ||||
| 2 | 2s | 2p | |||
| 3 | 3s | 3p | |||
| 4 | 4s | 3d | 4p | ||
| 5 | 5s | 4d | 5p | ||
| 6 | 6s | 4f | 5d | 6p | |
| 7 | 7s | 5f | 6d | 7p | |
| 8 | 8s | 5g | 6f | 7d | 8p |
Minħabba li l-elettroni ta' barra nett jiddeterminaw il-propjetajiet kimiċi, dawk l-elementi li għandhom l-istess numru t'elettroni tal-valenza huma fl-istess grupp tat-tavla.
Nimxu mill-eħfef element sal-itqal element, l-elettroni tal-qoxra ta' barra nett(dawk l-aktar aċċessibli għall-parteċipazzjoni f'reazzjonijiet kimiċi) huma kollha fl-istess tip t'orbital, b'forma simili, imma b'aktar enerġija u b'distanza ikbar min-nukleju. Pereżempju, l-elettroni fil-qoxra ta' barra (tal-valenza) tal-elementi fl-ewwel grupp, bl-Idroġenu fuq nett, kollha għandhom elettron wieħed f'orbital s. Fl-Idroġenu, dak l-orbital s hu l-aktar stat t'enerġija baxx possibli għal kwalunkwe atomu, l-orbital tal-eweel qoxra(rappreżentat mill-pożizzjoni tal-Idroġenu fl-ewwel perjodu tat-tavla). Fil-Franċju, l-aktar element tqil tal-grupp, fil-qoxra ta' barra nett l-elettroni huma fis-seba' orbital, sinnifikament aktar 'l barra min-nukleju minn dawk l-elettroni li jimlew il-qxur ta' taħha fl-enerġija. Bħalha eżempju ieħor, il-Karbonju u ċ-Ċomb għandhom 4 elettroni fl-orbitali tal-qoxra ta' barra.
Innota illi meta n-numru atomiku jiżdied (i.e. ċ-ċarġ fuq in-nukleju atomiku) , dan iwassal għal aktar "spin orbit coupling" bejn in-nukleju u l-elettroni, dan inaqqas il-validità tal-mudell tal-approssimazzjoni tal-orbital tal-mekkanika kwantistika, illi jikkunsidra kull orbital atomiku bħala entità separata.
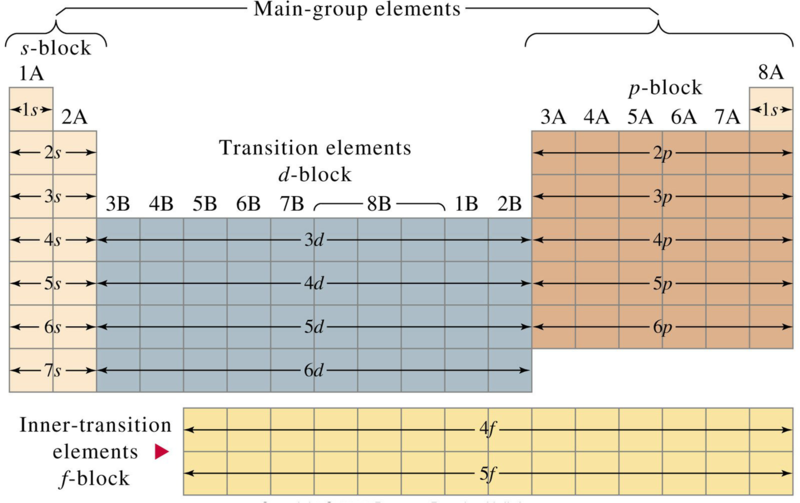
Minħabba l-importanza tal-qoxra ta' barra nett, ir-reġjuni differenti tat-tavla perjodika huma ġielu rriferuti bħala blokok tat-tavla perjodika, msemmija skont l-isem tas-sottoqoxra li fih l-aħħar elettron jinsab, e.ż. il-blokka s, il-blokka p, il-blokka d-block, eċċ.
Rigward l-elementi Ununbju, Ununtrju, Ununkwadju eċċ., huma elementi li ġew skoperti , imma s'issa għad m'għandhomx isem.
Storja
[immodifika | immodifika s-sors]Fil-Greċja Antika, il-filosfu Grieg Aristotle propona illi kien hemm erba' elementi prinċipali: l-arja, in-nar, l-art u l-ilma. Dawn l-elementi kollha setgħu jiġu mġiegħela jirreaġixxu flimkien biex joħolqu element ieħor; pereż., l-art u n-nar jinagħqdu flimkien biex jiffurmaw il-lava. Imma, din it-teorija intefgħet fil-ġenb meta l-elementi kimiċi vera bdew jiġu skoperti. Ix-Xjentisti kellhom bżonn databażi aċċessibli li fiha setgħet tiġi mniżżla u aċċeduta l-informazzjoni fuq l-elementi. Din kellha ssir magħrufa bħala t-Tavla Perjodika.
It-tavla oriġinali inħolqot qabel l-iskoperta tal-partiċelli subatomiċi jew il-formulazzjoni tat-teorija tal-mekkanika kwantistika kurrenti rigward l-istruttura atomika. Jekk wieħed jorganiżża l-elementi skont il-piż atomiku, u wara "jipplottja" propjetajiet oħrajn kontra l-piż atomiku, wieħed jinduna b'perjodiċità għal dawn il-propjetajiet bħala funzjoni tal-piż atomiku. L-ewwel persuna li għarfet dawn ir-regularitajiet kien il-kimiku Ġermaniż Johann Wolfgang Döbereiner li, fl-1829, induna b'numru ta' triadi t'elementi simili:
| Element | Piż Molari (g/mol) |
Densità (g/cm³) |
|---|---|---|
| Kloru | 35.453 | 0.0032 |
| Bromu | 79.904 | 3.1028 |
| Jodju | 126.90447 | 4.933 |
| Kalċju | 40.078 | 1.55 |
| Stronzju | 87.62 | 2.54 |
| Barju | 137.327 | 3.594 |
Fl-1829 Döbereiner ppropona l-Liġi tat-Triadi: L-element tan-nofs fit-triadu għandu l-piż atomiku li hu nofs l-piż tat-tnejn l-oħra flimkien(average). Id-densitajiet ta' xi triadi mxew ma tendenzi simili. Wara xjentisti oħrajn sabu relazzjonijiet kimiċi li jestendu 'l-bogħod mit-triadi. Il-Fluworu ġie miżjud mal-grupp ta' Cl/Br/I; iż-Żolfu, l-Ossiġenu, s-Selenju u t-Tellurju ġew gruppati f' familja; l-Ażotu, l-Fosfru, l-Arseniku, l-Antimonju, u l- Bismut ġew klassifikati bħala grupp ieħor.


Dan ġie segwit mill-kimiku Ingliż John Alexander Reina Newlands, illi fl-1865 innota li meta l-elementi jiġi ordnati skont il-piż atomiku tagħhom, elementi li għandhom propjetajiet fiżiċi simili kienu jirrikorru f'intervalli ta' tmienja, li kienu jixbhu l-ottavi tal-musika, imma l-liġi tal-"ottavi" tiegħu ġiet ridikolata mill-kontemporarji tiegħu.
Imma, għalkemm kellha suċċess għal xi elementi, il-liġi tal-ottavi ta' Newland falliet għal żewġ raġunijiet:
- Ma kinitx valida għall-elementi li kellhom piż atomiku għola minn dak tal-Kalċju.
- Meta elementi oħrajn ġew skoperti, bħall-gassijiet nobbli(He, Ne, Ar), ma setgħux jiġu akkomodati fuq din it-tavla.
Finalment, fl-1869 il-professur tal-kimika Russu Dmitri Ivanovich Mendeleev u erbgħa xhur wara l-Ġermaniż Julius Lothar Meyer indipendentament żviluppaw l-ewwel tavla perjodika, u rranġaw l-elementi skont il-piż. Imma, Mendeleev ħareġ xi elementi 'l-barra mis-sekwenza tal-piż stretta biex ikun jista' jqabbilhom aħjar mal-propjetajiet tal-ġirien tagħhom fit-tavla, hu rranġa żbalji fil-valuri ta' xi piżijiet atomiċi , u pprediċi l-eżistenza u l-propjetajiet ta' ftit elementi ġodda fl-ispazji vojta tat-tavla tiegħu. Mendeleev kien aktar tard ivvendikat bl-iskoperta tal-istruttura elettronika tal-elementi tard fid-19 -il seklu u kmieni fl-20 seklu.
Provi li saru aktar kmieni biex jitfgħu lista l-elementi biex juru r-relazzjonijiet bejniethom (pereżempju minn John Alexander Reina Newlands) normalment kienu jinvolvu l-ordinazzjoni skont il-piż atomiku. Is-sigriet għal Mendeleev hu u jagħmel it-tavla kien li jpoġġi l-elementi biex juru propjetajiet kimiċi rikurrenti jew perjodiċi (anka jekk dan kien ifisser li xi wħud minnhom ma jkunux ordinati skont il-piż), u li jħalli vojt għall-elementi "mitlufin". Mendeleev uża t-tavla tiegħu biex jaqtal-propjetajiet ta' dawn l-elementi "mitlufin", u ħafna minnhom ġew skoperti u ffitjaw mal-predizzjonijiet.
